JSMO2022<日本臨床腫瘤大會2022> 非小細胞肺癌(NSCLC)術后阿替利珠單抗輔助治療的成果
IMpower010-III期試驗亞洲人群亞組結果
2021年美國臨床腫瘤學會(ASCO 2021)上,一項名為IMpower010的III期隨機對照試驗因驗證了阿替利珠單抗(Atezolizumab) 術后輔助治療在早期非小細胞肺癌(NSCLC)中的療效和安全性,顯著延長了無病生存期(DFS)而成為了熱門話題。該結果表明,以往的常規鉑類術后輔助化療無法充分改善早期非小細胞肺癌(NSCLC)的預后。2021年9月歐洲臨床腫瘤協會(ESMO 2021)對此也追加了一項補充分析(相關文章「術後補助アテゾ、切除済みNSCLCに著効」「【肺がん動畫座談會①】IMpower010試験を読み解く」。
在今年2 月 17 ~19 日舉行的第19屆日本臨床腫瘤協會上,來自日本靜岡縣癌癥中心呼吸內科主任醫師釼持広知教授發布了該試驗的亞洲人群的亞組分析結果。
《試驗方法》
【試驗對象】:腫瘤完全切除術后stage IB(腫瘤組織直徑4cm以上)~IIIA期的非小細胞肺癌(NSCLC)患者符合條件的受試者以 1:1的比例隨機分配到以下 2組:
【阿替利珠組】:507人
術后輔助化療1~4周期+阿替利珠單抗(1200mg/q21,最長16周期)
【BSC組】:498人
最佳支持治療(BSC)
【主要終點】以下群體的無病生存期(DFS)
群體①PD-L1>1%, II~IIIA期患者(阿替利珠組248人,BSC組228人)
群體②所有II~IIIA期患者(阿替利珠組442人,BSC組440人)
《試驗結果》
★中位隨訪 32.8 個月的 DFS 分層風險比 (HR)
群體①:0.66(95%CI 0.50~0.88,P=0.004)
群體②:0.79(95%CI 0.64~0.96,P=0.02)
根據該研究結果,美國食品藥品監督管理局(FDA)于去年10月宣布批準阿替利朱單抗作為PD-L1>1%的II-IIIA期非小細胞肺癌的術后輔助治療。日本也提交了批準申請(相關文章「アテゾリズマブ、NSCLC術後療法として承認申請」)。
《試驗結果》補充
此次報告為該試驗亞洲人群的亞組報告。
【受試者】亞洲人群(日本、中國、臺灣、韓國、香港)共計233人,占總受試者的23.2%。阿替利珠組125人,BSC 組 108人,兩組患者背景無差異。男性比例低于總體人群,非吸煙者較多,非鱗癌,IIIA期,肺葉切除術,表皮生長因子受體(EGFR)基因突變率高。
★中位隨訪 32.5個月的 DFS 分層風險比 (HR)
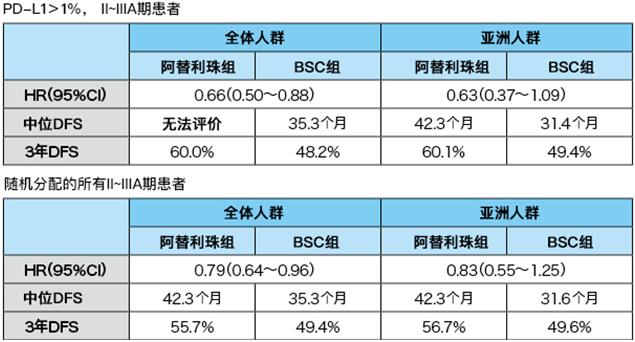
群體①:0.63(95%CI 0.37~1.09)
群體②:0.83(95%CI 0.55~1.25)
與全體患者人群結果相同。次要終點的總生存期OS也同樣不成熟。
(表)全體人群與亞洲人群PDF對比
★不良事件
也與全體患者人群的結果基本一致。值得注意的是:在亞洲人群中,阿替利珠組的肝炎、皮疹和肺炎的發生率很高,但大多數為 1/2 級。
綜上所述,釼持広知教授表示,“通過對亞洲人群的亞組分析,阿替利珠單抗對 PD-L1 陽性II-IIIA期NSCLC術后輔助治療的療效和安全性與全體患者人群抑制。”
即:即使在亞洲人群,相比最佳支持治療(BSC),輔助化療使用阿替利珠單抗也同樣能改善非小細胞肺癌術后 DFS。


