CAF分泌的TGF-β與口腔癌的惡性程度密切相關(guān) - 新潟大學(xué)
CAFs和癌細(xì)胞是如何相互影響的?
新潟大學(xué)10月7日宣布,它發(fā)現(xiàn)癌癥相關(guān)成纖維細(xì)胞(CAFs)的存在在口腔癌的發(fā)展中很重要。 這項(xiàng)研究是由該大學(xué)醫(yī)學(xué)和牙科研究生院的牙醫(yī)Kenta Haga博士、該大學(xué)口腔病理學(xué)系的講師Manabu Yamazaki、Junichi Tanuma等人領(lǐng)導(dǎo)的研究小組以及該大學(xué)組織工程和再生系的教授Kenji Izumi進(jìn)行的。 該研究結(jié)果已在線發(fā)表在《轉(zhuǎn)化腫瘤學(xué)》上。
口腔是人體中最重要的器官之一,因?yàn)樗哂羞M(jìn)食、吞咽和發(fā)音等功能。 因此,口腔癌的術(shù)后過(guò)程會(huì)對(duì)病人的尊嚴(yán)和生活質(zhì)量產(chǎn)生重大影響。
在之前的一項(xiàng)研究中,該研究小組調(diào)查了手術(shù)切除的組織,并報(bào)告說(shuō)SOX9在癌細(xì)胞中的表達(dá)與預(yù)后不良有關(guān),而且SOX9可以作為口腔癌等級(jí)的一個(gè)指標(biāo)。 近年來(lái),人們也很清楚,在各種癌癥中,構(gòu)成癌細(xì)胞周圍微環(huán)境的CAFs會(huì)影響癌癥的惡性程度。 然而,CAFs和癌細(xì)胞之間如何相互作用仍有待闡明。
同時(shí)服用TGF-β選擇性抑制劑可抑制小鼠腫瘤的形成
首先,該研究小組成功地創(chuàng)建了一個(gè)由CAFs和口腔癌細(xì)胞組成的3D體外模型。 與正常的口腔粘膜成纖維細(xì)胞(NOFs)相比,該模型顯示出增加的深層侵襲/遷移,表明癌細(xì)胞的惡性程度,以及癌細(xì)胞中更高的SOX9表達(dá)。
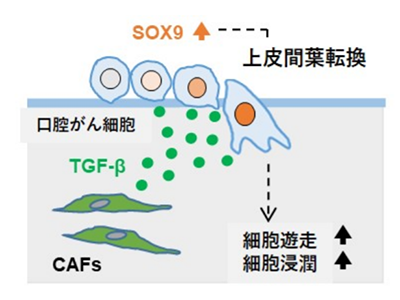
這個(gè)實(shí)驗(yàn)?zāi)P捅砻鳎珻AFs分泌的TGF-β深度參與了SOX9表達(dá)的增加和癌細(xì)胞的侵襲/遷移,而且CAFs分泌的TGF-β誘導(dǎo)上皮-間質(zhì)轉(zhuǎn)化為癌癥。
為了進(jìn)一步驗(yàn)證三維體外模型在個(gè)體水平上的結(jié)果,將口腔癌細(xì)胞與CAF或NOF混合后皮下移植到免疫力低下的小鼠體內(nèi)。 結(jié)果顯示,CAF共同移植組的腫瘤形成量是NOF組的兩倍,但同時(shí)加入對(duì)TGF-β有選擇性的抑制劑可以抑制腫瘤的形成效果。
研究人員還分析了手術(shù)切除的人類癌癥組織,發(fā)現(xiàn)SOX9陽(yáng)性細(xì)胞水平高的口腔癌組織基質(zhì)中CAFs比例較高與CAFs水平高的口腔癌患者的復(fù)發(fā)率較高之間存在關(guān)聯(lián)。
CAF分泌中的TGF-β增加SOX9轉(zhuǎn)錄因子的表達(dá),誘導(dǎo)癌細(xì)胞的上皮-間質(zhì)轉(zhuǎn)化,并 "增加 "口腔癌細(xì)胞的惡性潛力
這項(xiàng)研究表明,TGF-β是癌癥基質(zhì)中CAFs分泌的一種生長(zhǎng)因子,能增加口腔癌細(xì)胞中SOX9轉(zhuǎn)錄因子的表達(dá),誘導(dǎo)癌細(xì)胞的上皮-間質(zhì)轉(zhuǎn)化,增加口腔癌細(xì)胞的惡性程度(侵襲和遷移潛力)。 這導(dǎo)致了TGF-β/SOX9軸對(duì)以前報(bào)道的SOX9陽(yáng)性細(xì)胞和病人預(yù)后之間的影響的證明。
該研究小組說(shuō),通過(guò)針對(duì)調(diào)節(jié)癌癥惡性轉(zhuǎn)化的CAFs以及這些細(xì)胞分泌的TGF-β,可以將癌癥組織周圍的微環(huán)境增加為癌癥治療的新目標(biāo),有可能應(yīng)用于與癌癥細(xì)胞靶向藥物相結(jié)合的新型療法的開(kāi)發(fā)。


